ஒரு மூலக்கூறின் சுதந்திரத்தின் டிகிரி எண்ணிக்கை. ஐசோபிராசஸ்கள்
ஒரு தெர்மோடைனமிக் அமைப்பின் நிலை சமன்பாடு. கிளாபிரான்-மெண்டலீவ் சமன்பாடு. சிறந்த எரிவாயு வெப்பமானி. மூலக்கூறு இயக்கக் கோட்பாட்டின் அடிப்படை சமன்பாடு. மூலக்கூறுகளின் சுதந்திரத்தின் அளவு முழுவதும் ஆற்றலின் சீரான விநியோகம். ஒரு சிறந்த வாயுவின் உள் ஆற்றல். வாயு மூலக்கூறுகளின் பயனுள்ள விட்டம் மற்றும் சராசரி இலவச பாதை. மூலக்கூறு இயக்கக் கோட்பாட்டின் பரிசோதனை உறுதிப்படுத்தல்.
வெப்ப இயக்கவியல் அமைப்பின் நிலையின் சமன்பாடு அமைப்பின் அளவுருக்களுக்கு இடையிலான உறவை விவரிக்கிறது. . மாநில அளவுருக்கள் அழுத்தம், அளவு, வெப்பநிலை, பொருளின் அளவு. பொதுவாக, மாநிலத்தின் சமன்பாடு என்பது செயல்பாட்டு சார்பு F (p,V,T) = 0 ஆகும்.
பெரும்பாலான வாயுக்களுக்கு, அனுபவம் காட்டுவது போல், அறை வெப்பநிலை மற்றும் சுமார் 10 5 Pa அழுத்தத்தில், மெண்டலீவ்-கிளாபிரான் சமன்பாடு :
பஅழுத்தம் (பா), வி- ஆக்கிரமிக்கப்பட்ட அளவு (மீ 3), ஆர்=8.31 J/molK - உலகளாவிய வாயு மாறிலி, T - வெப்பநிலை (K).
பொருளின் மச்சம்
- அவகாட்ரோவின் எண்ணிக்கைக்கு சமமான பல அணுக்கள் அல்லது மூலக்கூறுகளைக் கொண்ட பொருளின் அளவு  (12 கிராம் கார்பன் ஐசோடோப்பு 12 C இல் எத்தனை அணுக்கள் உள்ளன). விடுங்கள் மீ 0 - ஒரு மூலக்கூறின் நிறை (அணு), என்என்பது மூலக்கூறுகளின் எண்ணிக்கை
(12 கிராம் கார்பன் ஐசோடோப்பு 12 C இல் எத்தனை அணுக்கள் உள்ளன). விடுங்கள் மீ 0 - ஒரு மூலக்கூறின் நிறை (அணு), என்என்பது மூலக்கூறுகளின் எண்ணிக்கை 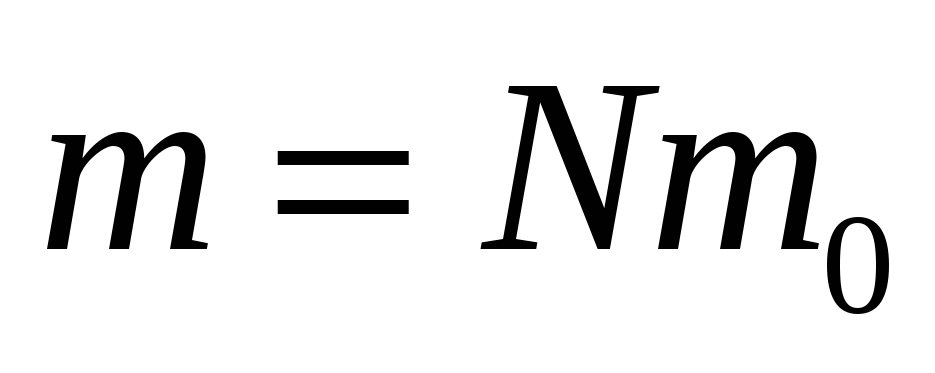 - வாயு நிறை,
- வாயு நிறை,  - பொருளின் மோலார் நிறை. எனவே, பொருளின் மோல்களின் எண்ணிக்கை இதற்கு சமம்:
- பொருளின் மோலார் நிறை. எனவே, பொருளின் மோல்களின் எண்ணிக்கை இதற்கு சமம்:
 .
.
Clapeyron-Mendeleev சமன்பாட்டை பூர்த்தி செய்யும் ஒரு வாயு ஒரு சிறந்த வாயு ஆகும். இலட்சியத்திற்கு மிக நெருக்கமான பண்புகள் ஹைட்ரஜன் மற்றும் ஹீலியம் ஆகும்.
சிறந்த எரிவாயு வெப்பமானி.
ஒரு நிலையான-தொகுதி வாயு வெப்பமானி ஒரு தெர்மோமெட்ரிக் உடலைக் கொண்டுள்ளது - ஒரு பாத்திரத்தில் மூடப்பட்ட ஒரு சிறந்த வாயுவின் ஒரு பகுதி, இது ஒரு குழாயைப் பயன்படுத்தி அழுத்த அளவோடு இணைக்கப்பட்டுள்ளது.
ஒரு எரிவாயு வெப்பமானியைப் பயன்படுத்தி, ஒரு குறிப்பிட்ட அளவுக்கான வாயு வெப்பநிலை மற்றும் வாயு அழுத்தத்திற்கு இடையேயான உறவை நீங்கள் சோதனை முறையில் நிறுவலாம். அழுத்த அளவின் இடது குழாயின் செங்குத்து இயக்கம், அதன் வலது குழாயில் உள்ள அளவை குறிப்பு குறிக்கு கொண்டு வருதல் மற்றும் அழுத்தம் அளவீட்டில் உள்ள திரவ நிலைகளின் உயரத்தில் உள்ள வேறுபாட்டை அளவிடுவதன் மூலம் தொகுதி நிலைத்தன்மை அடையப்படுகிறது. பல்வேறு திருத்தங்களை கணக்கில் எடுத்துக்கொள்வது (உதாரணமாக, தெர்மோமீட்டரின் கண்ணாடி பகுதிகளின் வெப்ப விரிவாக்கம், வாயு உறிஞ்சுதல் போன்றவை) 0.001 K க்கு சமமான நிலையான-அளவிலான வாயு வெப்பமானி மூலம் வெப்பநிலை அளவீட்டின் துல்லியத்தை அடைய முடியும்.
எரிவாயு வெப்பமானிகள் வெப்பநிலை அவற்றின் உதவியுடன் தீர்மானிக்கப்படும் நன்மையைக் கொண்டுள்ளன குறைந்த அடர்த்திவாயு அதன் இயல்பைச் சார்ந்து இல்லை, அத்தகைய வெப்பமானியின் அளவு ஒரு சிறந்த வாயு வெப்பமானியைப் பயன்படுத்தி நிர்ணயிக்கப்பட்ட முழுமையான வெப்பநிலை அளவோடு நன்றாக ஒத்துப்போகிறது.
இந்த வழியில், ஒரு குறிப்பிட்ட வெப்பநிலையானது டிகிரி செல்சியஸ் வெப்பநிலையுடன் தொடர்புடையது: 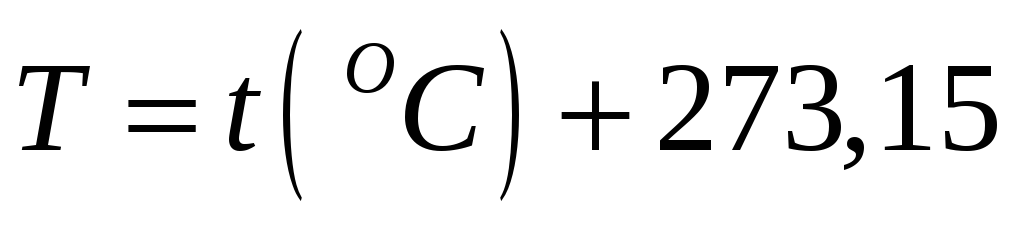 TO.
TO.
சாதாரண எரிவாயு நிலைமைகள் - அழுத்தம் சாதாரண வளிமண்டல அழுத்தத்திற்கு சமமாக இருக்கும் நிலை: ஆர்= 101325 Pa10 5 Pa மற்றும் வெப்பநிலை T = 273.15 K.
மெண்டலீவ்-கிளாபிரான் சமன்பாட்டிலிருந்து, சாதாரண நிலைமைகளின் கீழ் 1 மோல் வாயுவின் அளவு சமமாக இருக்கும்:  மீ 3.
மீ 3.
MKT இன் அடிப்படைகள்
மூலக்கூறு இயக்கவியல் கோட்பாடு (MKT) வாயுக்களின் வெப்ப இயக்கவியல் பண்புகளை அவற்றின் மூலக்கூறு கட்டமைப்பின் பார்வையில் இருந்து கருதுகிறது.
மூலக்கூறுகள் நிலையான, சீரற்ற வெப்ப இயக்கத்தில் உள்ளன, தொடர்ந்து ஒன்றோடொன்று மோதுகின்றன. அதே நேரத்தில், அவை வேகத்தையும் ஆற்றலையும் பரிமாறிக்கொள்கின்றன.
வாயு அழுத்தம்.
ஒரு பாத்திரத்தின் சுவர்களுடன் வெப்ப இயக்கவியல் சமநிலையில் ஒரு வாயுவின் இயந்திர மாதிரியைக் கருத்தில் கொள்வோம். மூலக்கூறுகள் மீள்தன்மையுடன் ஒன்றோடு ஒன்று மோதுகின்றன, ஆனால் வாயுவைக் கொண்ட பாத்திரத்தின் சுவர்களிலும் மோதுகின்றன.
மாதிரியின் சிறந்ததாக, மூலக்கூறுகளில் உள்ள அணுக்களை பொருள் புள்ளிகளுடன் மாற்றுகிறோம். அனைத்து மூலக்கூறுகளின் வேகமும் ஒரே மாதிரியாக இருக்கும் என்று கருதப்படுகிறது. பொருள் புள்ளிகள் ஒருவருக்கொருவர் தொலைவில் தொடர்பு கொள்ளாது என்று நாங்கள் கருதுகிறோம், எனவே அத்தகைய தொடர்புகளின் சாத்தியமான ஆற்றலை பூஜ்ஜியத்திற்கு சமமாக எடுத்துக்கொள்கிறோம்.
பி  Ust
Ust
 - வாயு மூலக்கூறுகளின் செறிவு, டி- வாயு வெப்பநிலை, u- மூலக்கூறுகளின் மொழிபெயர்ப்பு இயக்கத்தின் சராசரி வேகம். ஒரு ஒருங்கிணைப்பு அமைப்பைத் தேர்ந்தெடுப்போம், இதனால் கப்பலின் சுவர் XY விமானத்தில் உள்ளது, மேலும் Z அச்சு கப்பலின் உள்ளே சுவருக்கு செங்குத்தாக இயக்கப்படுகிறது.
- வாயு மூலக்கூறுகளின் செறிவு, டி- வாயு வெப்பநிலை, u- மூலக்கூறுகளின் மொழிபெயர்ப்பு இயக்கத்தின் சராசரி வேகம். ஒரு ஒருங்கிணைப்பு அமைப்பைத் தேர்ந்தெடுப்போம், இதனால் கப்பலின் சுவர் XY விமானத்தில் உள்ளது, மேலும் Z அச்சு கப்பலின் உள்ளே சுவருக்கு செங்குத்தாக இயக்கப்படுகிறது.
ஒரு பாத்திரத்தின் சுவர்களில் மூலக்கூறுகளின் தாக்கங்களைக் கருத்தில் கொள்வோம். ஏனெனில் தாக்கங்கள் மீள்தன்மை கொண்டவை, பின்னர் சுவரில் மோதிய பிறகு மூலக்கூறின் வேகம் திசையை மாற்றுகிறது, ஆனால் அதன் அளவு மாறாது.
ஒரு காலத்தில் டிதொலைவில் சுவரில் இருந்து அமைந்துள்ள மூலக்கூறுகள் மட்டுமே எல்= uடி. அடிப்படை பரப்பளவைக் கொண்ட சிலிண்டரில் உள்ள மூலக்கூறுகளின் மொத்த எண்ணிக்கை எஸ்மற்றும் உயரம் எல், இதன் அளவு சமம் வி = எல்.எஸ். = uடிஎஸ், சமம் என் = nவி = nuடிஎஸ்.
விண்வெளியில் கொடுக்கப்பட்ட புள்ளியில், மூலக்கூறு இயக்கத்தின் மூன்று வெவ்வேறு திசைகளை நாம் நிபந்தனையுடன் வேறுபடுத்தலாம், எடுத்துக்காட்டாக, X, Y, Z அச்சுகள். ஒரு மூலக்கூறு "முன்னோக்கி" மற்றும் "பின்னோக்கி" ஒவ்வொரு திசையிலும் நகரும்.
எனவே, ஒதுக்கப்பட்ட தொகுதியில் உள்ள அனைத்து மூலக்கூறுகளும் சுவரை நோக்கி நகராது, ஆனால் அவற்றின் மொத்த எண்ணிக்கையில் ஆறில் ஒரு பங்கு மட்டுமே. எனவே, அந்த நேரத்தில் மூலக்கூறுகளின் எண்ணிக்கை டிசுவரைத் தாக்கினால், அது சமமாக இருக்கும்:
என் 1 = என்/6= nuடிஎஸ்/6.
தாக்கத்தின் போது மூலக்கூறுகளின் வேகத்தில் ஏற்படும் மாற்றம் சுவரின் பக்கத்திலிருந்து மூலக்கூறுகளில் செயல்படும் சக்தியின் தூண்டுதலுக்கு சமம் - அதே அளவு சக்தியுடன் மூலக்கூறுகள் சுவரில் செயல்படுகின்றன:
பி Z = பி 2 Z – பி 1 Z = எஃப்டி, அல்லது
என் 1 மீ 0 நீ -( என் 1 மீ 0 u)= எஃப்டி,
2என் 1 மீ 0 u = Fடி,
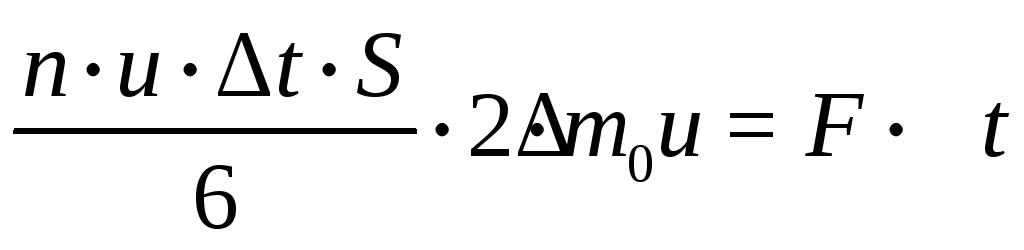 ,
,
 .
.
சுவரில் வாயு அழுத்தத்தை எங்கே காணலாம்:  ,
,
எங்கே  - ஒரு பொருள் புள்ளியின் இயக்க ஆற்றல் (ஒரு மூலக்கூறின் மொழிபெயர்ப்பு இயக்கம்). இதன் விளைவாக, அத்தகைய (இயந்திர) வாயுவின் அழுத்தம் மூலக்கூறுகளின் மொழிபெயர்ப்பு இயக்கத்தின் இயக்க ஆற்றலுக்கு விகிதாசாரமாகும்:
- ஒரு பொருள் புள்ளியின் இயக்க ஆற்றல் (ஒரு மூலக்கூறின் மொழிபெயர்ப்பு இயக்கம்). இதன் விளைவாக, அத்தகைய (இயந்திர) வாயுவின் அழுத்தம் மூலக்கூறுகளின் மொழிபெயர்ப்பு இயக்கத்தின் இயக்க ஆற்றலுக்கு விகிதாசாரமாகும்:
 .
.
இந்த சமன்பாடு அழைக்கப்படுகிறது அடிப்படை MKT சமன்பாடு .
சுதந்திரத்தின் அளவுகளில் ஆற்றல் சீரான விநியோகம் சட்டம் .
வெப்ப இயக்கவியலின் அடிப்படைக் கருத்துக்கள்.
MCT போலல்லாமல், வெப்ப இயக்கவியல் உடல்கள் மற்றும் இயற்கை நிகழ்வுகளின் மேக்ரோஸ்கோபிக் பண்புகளை அவற்றின் நுண்ணிய படத்தில் ஆர்வம் காட்டாமல் ஆய்வு செய்கிறது. அணுக்கள் மற்றும் மூலக்கூறுகளை கருத்தில் கொள்ளாமல், செயல்முறைகளின் நுண்ணிய ஆய்வுக்குள் நுழையாமல், வெப்ப இயக்கவியல் ஒருவரை அவற்றின் நிகழ்வு குறித்து பல முடிவுகளை எடுக்க அனுமதிக்கிறது.
வெப்ப இயக்கவியல் என்பது பல அடிப்படைச் சட்டங்களை அடிப்படையாகக் கொண்டது (வெப்ப இயக்கவியலின் கொள்கைகள் என அழைக்கப்படுகிறது), இது ஒரு பெரிய அளவிலான சோதனை உண்மைகளின் பொதுமைப்படுத்தலின் அடிப்படையில் நிறுவப்பட்டது.
பல்வேறு கோணங்களில் இருந்து பொருளின் நிலையில் ஏற்படும் மாற்றங்களைக் கருத்தில் கொண்டு, வெப்ப இயக்கவியல் மற்றும் MCT ஆகியவை ஒன்றையொன்று பூர்த்தி செய்து, அடிப்படையில் ஒரு முழுமையை உருவாக்குகின்றன.
வெப்ப இயக்கவியல்- தெர்மோடைனமிக் சமநிலையின் நிலையில் உள்ள மேக்ரோஸ்கோபிக் அமைப்புகளின் பொதுவான பண்புகள் மற்றும் இந்த நிலைகளுக்கு இடையிலான மாற்றத்தின் செயல்முறைகளைப் படிக்கும் இயற்பியலின் ஒரு பிரிவு.
வெப்ப இயக்கவியல் முறைஆற்றல் என்ற கருத்தின் அறிமுகத்தை அடிப்படையாகக் கொண்டது மற்றும் ஆற்றல் பார்வையில் இருந்து செயல்முறைகளை கருதுகிறது, அதாவது, ஆற்றல் பாதுகாப்பு விதி மற்றும் ஒரு வகையிலிருந்து மற்றொரு வகைக்கு அதன் மாற்றம் ஆகியவற்றின் அடிப்படையில்.
வெப்ப இயக்கவியல் அமைப்பு- ஒருவருக்கொருவர் மற்றும் வெளிப்புற சூழலுடன் ஆற்றலை பரிமாறிக்கொள்ளக்கூடிய உடல்களின் தொகுப்பு.
வெப்ப இயக்கவியல் அமைப்பை விவரிக்க, உடல் அளவுகள் அறிமுகப்படுத்தப்படுகின்றன, அவை வெப்ப இயக்கவியல் அளவுருக்கள் அல்லது கணினி நிலை அளவுருக்கள் என்று அழைக்கப்படுகின்றன: p,V,T.
வெப்ப இயக்கவியல் அமைப்பின் நிலையை வகைப்படுத்தும் இயற்பியல் அளவுகள் அழைக்கப்படுகின்றன வெப்ப இயக்கவியல் அளவுருக்கள்.
அழுத்தம்இயற்பியல் அளவு என்பது இந்த மேற்பரப்பிற்கு இயல்பான திசையில் உடலின் ஒரு யூனிட் பரப்பளவிற்கு செயல்படும் விசைக்கு எண்ணியல் ரீதியாக சமம்: , ![]() .
.
சாதாரண வளிமண்டல அழுத்தம் 1 atm = 10 5 Pa ஆகும்.
முழுமையான வெப்பநிலை- மூலக்கூறுகளின் சராசரி இயக்க ஆற்றலின் அளவீடு.
![]() .
.
வெப்ப இயக்கவியல் அமைப்பு அமைந்துள்ள நிலைகள் வேறுபட்டிருக்கலாம்.
கணினியின் வெவ்வேறு புள்ளிகளில் உள்ள அளவுருக்களில் ஒன்று ஒரே மாதிரியாக இல்லாமல் காலப்போக்கில் மாறினால், அமைப்பின் இந்த நிலை அழைக்கப்படுகிறது சமநிலையற்றது.
அனைத்து தெர்மோடைனமிக் அளவுருக்கள் தன்னிச்சையாக நீண்ட காலத்திற்கு அமைப்பின் அனைத்து புள்ளிகளிலும் மாறாமல் இருந்தால், அத்தகைய நிலை அழைக்கப்படுகிறது சமநிலை, அல்லது தெர்மோடைனமிக் சமநிலையின் நிலை.
எந்தவொரு மூடிய அமைப்பும், ஒரு குறிப்பிட்ட நேரத்திற்குப் பிறகு, தன்னிச்சையாக ஒரு சமநிலை நிலைக்கு செல்கிறது.
குறைந்தபட்சம் அதன் அளவுருக்களில் ஏதேனும் ஒரு மாற்றத்துடன் தொடர்புடைய அமைப்பின் நிலையில் எந்த மாற்றமும் அழைக்கப்படுகிறது வெப்ப இயக்கவியல் செயல்முறை.ஒவ்வொரு அடுத்தடுத்த நிலையும் முந்தைய நிலையிலிருந்து எண்ணற்ற அளவில் வேறுபடும் ஒரு செயல்முறை, அதாவது. சமநிலை நிலைகளின் வரிசையை பிரதிபலிக்கிறது, இது சமநிலை எனப்படும்.
அனைத்து சமநிலை செயல்முறைகளும் முடிவில்லாமல் மெதுவாக தொடர்கின்றன என்பது வெளிப்படையானது.
சமநிலை செயல்முறை எதிர் திசையில் மேற்கொள்ளப்படலாம், மேலும் கணினி முன்னோக்கி செயல்பாட்டின் போது அதே நிலைகள் வழியாக செல்லும், ஆனால் தலைகீழ் வரிசையில். எனவே, சமநிலை செயல்முறைகள் அழைக்கப்படுகின்றன மீளக்கூடியது.
ஒரு அமைப்பு, தொடர்ச்சியான மாற்றங்களுக்குப் பிறகு, அதன் அசல் நிலைக்குத் திரும்பும் செயல்முறை அழைக்கப்படுகிறது வட்ட செயல்முறைஅல்லது மிதிவண்டி.
வெப்ப இயக்கவியலின் அனைத்து அளவு முடிவுகளும் கண்டிப்பாக சமநிலை நிலைகள் மற்றும் மீளக்கூடிய செயல்முறைகளுக்கு மட்டுமே பொருந்தும்.
ஒரு மூலக்கூறின் சுதந்திரத்தின் டிகிரி எண்ணிக்கை. சுதந்திரத்தின் அளவுகளில் ஆற்றலின் சீரான விநியோகத்தின் சட்டம்.
சுதந்திரத்தின் அளவுகளின் எண்ணிக்கை- விண்வெளியில் அமைப்பின் நிலையை முழுமையாக தீர்மானிக்கும் சுயாதீன ஆயங்களின் எண்ணிக்கை. ஒரு மோனாடோமிக் வாயு மூலக்கூறு மூன்று டிகிரி மொழிபெயர்ப்பு இயக்கத்தின் சுதந்திரத்துடன் ஒரு பொருள் புள்ளியாகக் கருதப்படலாம்.
ஒரு டையட்டோமிக் வாயு மூலக்கூறு என்பது சிதைக்க முடியாத பிணைப்பால் கடுமையாக இணைக்கப்பட்ட இரண்டு பொருள் புள்ளிகளின் (அணுக்கள்) தொகுப்பாகும்; மொழிபெயர்ப்பு இயக்கத்தின் மூன்று டிகிரி சுதந்திரத்துடன் கூடுதலாக, இது சுழற்சி இயக்கத்தின் சுதந்திரத்தின் மேலும் இரண்டு டிகிரிகளைக் கொண்டுள்ளது (படம் 1).
ட்ரை- மற்றும் பாலிடோமிக் மூலக்கூறுகள் 3+3=6 டிகிரி சுதந்திரத்தைக் கொண்டுள்ளன (படம் 1).
இயற்கையாகவே, அணுக்களுக்கு இடையே உறுதியான தொடர்பு இல்லை. எனவே, உண்மையான மூலக்கூறுகளுக்கு, அதிர்வு இயக்கத்தின் சுதந்திரத்தின் அளவுகள் (மோனாடோமிக் தவிர) கணக்கில் எடுத்துக்கொள்ளப்பட வேண்டும்.
 |
காட்டப்பட்டுள்ளபடி, ஒரு மூலக்கூறின் மொழிபெயர்ப்பு இயக்கத்தின் சராசரி இயக்க ஆற்றல் சமம்
சுதந்திரத்தின் அளவுகளின் எண்ணிக்கைவிண்வெளியில் உடலின் நிலையை தீர்மானிக்க உள்ளிடப்பட வேண்டிய மிகச்சிறிய எண்ணிக்கையிலான சுயாதீன ஆயத்தொலைவு ஆகும். - சுதந்திரத்தின் அளவுகளின் எண்ணிக்கை.
கருத்தில் கொள்வோம் மோனாடோமிக் வாயு. அத்தகைய வாயுவின் மூலக்கூறை ஒரு பொருள் புள்ளியாகக் கருதலாம், பொருள் புள்ளியின் நிலை  விண்வெளியில் (படம் 11.1) மூன்று ஆயங்களால் தீர்மானிக்கப்படுகிறது.
விண்வெளியில் (படம் 11.1) மூன்று ஆயங்களால் தீர்மானிக்கப்படுகிறது.
மூலக்கூறு மூன்று திசைகளில் நகர முடியும் (படம் 11.2).
|
|
|
இதன் விளைவாக, இது மூன்று மொழிப்பெயர்ப்பு அளவு சுதந்திரத்தைக் கொண்டுள்ளது.
ஒரு மூலக்கூறு என்பது ஒரு பொருள் புள்ளி.
சுழற்சி இயக்கத்தின் ஆற்றல்  , ஏனெனில் புள்ளி வழியாக செல்லும் அச்சுடன் தொடர்புடைய ஒரு பொருள் புள்ளியின் நிலைமத்தின் தருணம் பூஜ்ஜியமாகும்
, ஏனெனில் புள்ளி வழியாக செல்லும் அச்சுடன் தொடர்புடைய ஒரு பொருள் புள்ளியின் நிலைமத்தின் தருணம் பூஜ்ஜியமாகும் 
ஒரு மோனாடோமிக் வாயு மூலக்கூறுக்கு, சுதந்திரத்தின் அளவுகளின் எண்ணிக்கை  .
.
கருத்தில் கொள்வோம் இரு அணு வாயு. ஒரு டையடோமிக் மூலக்கூறில், ஒவ்வொரு அணுவும் ஒரு பொருள் புள்ளியாக எடுத்துக் கொள்ளப்படுகிறது, மேலும் அணுக்கள் ஒன்றுக்கொன்று இறுக்கமாக இணைக்கப்பட்டுள்ளன என்று நம்பப்படுகிறது; இது ஒரு டயட்டோமிக் மூலக்கூறின் டம்பல் மாதிரி. டயட்டோமிக் இறுக்கமாக பிணைக்கப்பட்ட மூலக்கூறு(சிதைக்க முடியாத இணைப்பால் இணைக்கப்பட்ட இரண்டு பொருள் புள்ளிகளின் தொகுப்பு), படம். 11.3.
மூலக்கூறின் வெகுஜன மையத்தின் நிலை மூன்று ஆயங்களால் குறிப்பிடப்படுகிறது, (படம் 11.4) இவை மூன்று டிகிரி சுதந்திரம், அவை தீர்மானிக்கின்றன ஒரு மூலக்கூறின் மொழிபெயர்ப்பு இயக்கம்.ஆனால் மூலக்கூறு அதன் அச்சுகளைச் சுற்றி சுழற்சி இயக்கங்களையும் செய்ய முடியும்  மற்றும்
மற்றும்  , இவை மேலும் இரண்டு டிகிரி சுதந்திரத்தை தீர்மானிக்கின்றன மூலக்கூறு சுழற்சி. ஒரு அச்சைச் சுற்றி ஒரு மூலக்கூறின் சுழற்சி
, இவை மேலும் இரண்டு டிகிரி சுதந்திரத்தை தீர்மானிக்கின்றன மூலக்கூறு சுழற்சி. ஒரு அச்சைச் சுற்றி ஒரு மூலக்கூறின் சுழற்சி  சாத்தியமற்றது, ஏனெனில் பொருள் புள்ளிகள் இந்த புள்ளிகள் வழியாக ஒரு அச்சில் சுழற்ற முடியாது.
சாத்தியமற்றது, ஏனெனில் பொருள் புள்ளிகள் இந்த புள்ளிகள் வழியாக ஒரு அச்சில் சுழற்ற முடியாது.
|
|
|
ஒரு டையட்டோமிக் வாயு மூலக்கூறுக்கு, சுதந்திரத்தின் அளவுகளின் எண்ணிக்கை  .
.
கருத்தில் கொள்வோம் முக்கோண வாயு.ஒரு மூலக்கூறின் மாதிரியானது மூன்று அணுக்கள் (பொருள் புள்ளிகள்), ஒருவருக்கொருவர் கடுமையாக இணைக்கப்பட்டுள்ளது (படம் 11.5).
ஒரு முக்கோண மூலக்கூறு இறுக்கமாக பிணைக்கப்பட்ட மூலக்கூறு ஆகும்.
ஒரு முக்கோண வாயு மூலக்கூறுக்கு, சுதந்திரத்தின் அளவுகளின் எண்ணிக்கை  .
.
ஒரு பாலிடோமிக் மூலக்கூறுக்கு, சுதந்திரத்தின் அளவுகளின் எண்ணிக்கை  .
.
அணுக்களுக்கு இடையே உறுதியான பிணைப்புகள் இல்லாத உண்மையான மூலக்கூறுகளுக்கு, அதிர்வு இயக்கத்தின் சுதந்திரத்தின் அளவுகளை கணக்கில் எடுத்துக்கொள்வது அவசியம், பின்னர் ஒரு உண்மையான மூலக்கூறின் சுதந்திரத்தின் அளவுகளின் எண்ணிக்கை சமமாக இருக்கும்.
நான்= நான்+ பொருந்தும் நான்சுழற்று + நான்அலைவு (11.1)
சுதந்திரத்தின் அளவுகளுக்கு மேல் ஆற்றல் சீரான விநியோகம் சட்டம் (போல்ட்ஸ்மேனின் சட்டம்)
சுதந்திரத்தின் அளவுகளில் ஆற்றலின் சமநிலைப் பகிர்வு பற்றிய சட்டம்துகள்களின் அமைப்பு வெப்ப இயக்கவியல் சமநிலையில் இருந்தால், 1 டிகிரி சுதந்திரத்திற்கு மூலக்கூறுகளின் குழப்பமான இயக்கத்தின் சராசரி இயக்க ஆற்றல் மொழிபெயர்ப்பு மற்றும் சுழற்சிஇயக்கம் சமம் 
எனவே, ஒரு மூலக்கூறு உள்ளது  சுதந்திரத்தின் அளவு, ஆற்றல் உள்ளது
சுதந்திரத்தின் அளவு, ஆற்றல் உள்ளது
 , (11.2)
, (11.2)
எங்கே  - போல்ட்ஸ்மேன் நிலையான;
- போல்ட்ஸ்மேன் நிலையான;  - முழுமையான வாயு வெப்பநிலை.
- முழுமையான வாயு வெப்பநிலை.
உள் ஆற்றல்  சிறந்த வாயுஅதன் அனைத்து மூலக்கூறுகளின் இயக்க ஆற்றல்களின் கூட்டுத்தொகை ஆகும்.
சிறந்த வாயுஅதன் அனைத்து மூலக்கூறுகளின் இயக்க ஆற்றல்களின் கூட்டுத்தொகை ஆகும்.
உள் ஆற்றலைக் கண்டறிதல்  ஒரு சிறந்த வாயுவின் ஒரு மோல்.
ஒரு சிறந்த வாயுவின் ஒரு மோல்.  , எங்கே
, எங்கே  - ஒரு வாயு மூலக்கூறின் சராசரி இயக்க ஆற்றல்,
- ஒரு வாயு மூலக்கூறின் சராசரி இயக்க ஆற்றல்,  - அவகாட்ரோ எண் (ஒரு மோலில் உள்ள மூலக்கூறுகளின் எண்ணிக்கை). போல்ட்ஸ்மேனின் நிலையானது
- அவகாட்ரோ எண் (ஒரு மோலில் உள்ள மூலக்கூறுகளின் எண்ணிக்கை). போல்ட்ஸ்மேனின் நிலையானது  . பிறகு
. பிறகு
ஒரு வாயு நிறை இருந்தால்  , அந்த
, அந்த  - மோல்களின் எண்ணிக்கை, எங்கே
- மோல்களின் எண்ணிக்கை, எங்கே  மோலின் நிறை மற்றும் வாயுவின் உள் ஆற்றல் சூத்திரத்தால் வெளிப்படுத்தப்படுகிறது
மோலின் நிறை மற்றும் வாயுவின் உள் ஆற்றல் சூத்திரத்தால் வெளிப்படுத்தப்படுகிறது
 . (11.3)
. (11.3)
ஒரு சிறந்த வாயுவின் உள் ஆற்றல் வாயுவின் வெப்பநிலையை மட்டுமே சார்ந்துள்ளது. ஒரு சிறந்த வாயுவின் உள் ஆற்றலில் ஏற்படும் மாற்றம் வெப்பநிலையில் ஏற்படும் மாற்றத்தால் தீர்மானிக்கப்படுகிறது மற்றும் இந்த மாற்றம் நிகழ்ந்த செயல்முறையைப் பொறுத்தது அல்ல.
ஒரு சிறந்த வாயுவின் உள் ஆற்றலில் மாற்றம்
 , (11.4)
, (11.4)
எங்கே  - வெப்பநிலை மாற்றம்.
- வெப்பநிலை மாற்றம்.
ஒரு மூலக்கூறில் உள்ள அணுக்களின் அதிர்வு இயக்கத்திற்கு சீரான ஆற்றல் விநியோக விதி பொருந்தும். சுதந்திரத்தின் அதிர்வு அளவு இயக்க ஆற்றலுக்கு மட்டுமல்ல, சாத்தியமான ஆற்றலுக்கும் காரணமாகிறது, மேலும் ஒரு டிகிரிக்கு இயக்க ஆற்றலின் சராசரி மதிப்பு ஒரு டிகிரி சுதந்திரத்திற்கான சாத்தியமான ஆற்றலின் சராசரி மதிப்புக்கு சமமாக இருக்கும். 
எனவே, ஒரு மூலக்கூறுக்கு பல அளவு சுதந்திரம் இருந்தால் நான்= நான்+ பொருந்தும் நான்சுழற்று + நான்அதிர்வுகள், பின்னர் மூலக்கூறின் சராசரி மொத்த ஆற்றல்:  , மற்றும் வாயு வெகுஜனத்தின் உள் ஆற்றல்
, மற்றும் வாயு வெகுஜனத்தின் உள் ஆற்றல்  :
:
 . (11.5)
. (11.5)
| " |
தெர்மோடைனமிக்ஸின் இயற்பியல் அடிப்படைகள்
1. வெப்ப இயக்கவியலின் முதல் விதி
§1. உள் ஆற்றல்
எந்தவொரு மாநிலத்திலும் உள்ள எந்த வெப்ப இயக்க முறைமையும் ஆற்றல் கொண்டது, இது மொத்த ஆற்றல் என்று அழைக்கப்படுகிறது. அமைப்பின் மொத்த ஆற்றல், ஒட்டுமொத்த அமைப்பின் இயக்கத்தின் இயக்க ஆற்றல், ஒட்டுமொத்த அமைப்பின் சாத்தியமான ஆற்றல் மற்றும் உள் ஆற்றல் ஆகியவற்றைக் கொண்டுள்ளது.
 ஒரு அமைப்பின் உள் ஆற்றல் மூலக்கூறுகளின் அனைத்து வகையான குழப்பமான (வெப்ப) இயக்கத்தின் கூட்டுத்தொகையைக் குறிக்கிறது: உள்-அணு மற்றும் உள்-அணு இயக்கங்களிலிருந்து சாத்தியமான ஆற்றல். உள் ஆற்றல் என்பது வாயு நிலையின் செயல்பாடாகும். ஒரு வாயுவின் கொடுக்கப்பட்ட நிலைக்கு, உள் ஆற்றல் தனித்துவமாக தீர்மானிக்கப்படுகிறது, அதாவது, இது ஒரு குறிப்பிட்ட செயல்பாடு.
ஒரு அமைப்பின் உள் ஆற்றல் மூலக்கூறுகளின் அனைத்து வகையான குழப்பமான (வெப்ப) இயக்கத்தின் கூட்டுத்தொகையைக் குறிக்கிறது: உள்-அணு மற்றும் உள்-அணு இயக்கங்களிலிருந்து சாத்தியமான ஆற்றல். உள் ஆற்றல் என்பது வாயு நிலையின் செயல்பாடாகும். ஒரு வாயுவின் கொடுக்கப்பட்ட நிலைக்கு, உள் ஆற்றல் தனித்துவமாக தீர்மானிக்கப்படுகிறது, அதாவது, இது ஒரு குறிப்பிட்ட செயல்பாடு.
ஒரு மாநிலத்திலிருந்து மற்றொரு நிலைக்கு மாறும்போது, அமைப்பின் உள் ஆற்றல் மாறுகிறது. ஆனால் அதே நேரத்தில், புதிய நிலையில் உள்ள உள் ஆற்றல் அமைப்பு இந்த நிலைக்குச் செல்லும் செயல்முறையைப் பொறுத்தது அல்ல.
§2. வெப்பம் மற்றும் வேலை
வெப்ப இயக்கவியல் அமைப்பின் உள் ஆற்றலை மாற்ற இரண்டு வெவ்வேறு வழிகள் உள்ளன. ஒரு அமைப்பின் உள் ஆற்றல், செய்யப்படும் வேலையின் விளைவாகவும், கணினிக்கு வெப்ப பரிமாற்றத்தின் விளைவாகவும் மாறலாம். வேலை என்பது ஒரு அமைப்பின் இயந்திர ஆற்றலில் ஏற்படும் மாற்றத்தின் அளவீடு ஆகும். வேலை செய்யும் போது, கணினி அல்லது தனிப்பட்ட மேக்ரோஸ்கோபிக் பாகங்கள் ஒருவருக்கொருவர் தொடர்புடையதாக நகரும். எடுத்துக்காட்டாக, ஒரு பிஸ்டனை வாயுவைக் கொண்ட உருளைக்குள் தள்ளுவதன் மூலம், வாயுவை அழுத்துகிறோம், இதன் விளைவாக அதன் வெப்பநிலை அதிகரிக்கிறது, அதாவது. வாயுவின் உள் ஆற்றல் மாறுகிறது.
வெப்ப பரிமாற்றத்தின் விளைவாக உள் ஆற்றல் மாறலாம், அதாவது. வாயுவிற்கு சிறிது வெப்பத்தை கொடுக்கிறதுகே.
வெப்பத்திற்கும் வேலைக்கும் உள்ள வேறுபாடு என்னவென்றால், பல நுண்ணிய செயல்முறைகளின் விளைவாக வெப்பம் மாற்றப்படுகிறது, இதில் மோதல்களின் போது வெப்பமான உடலின் மூலக்கூறுகளின் இயக்க ஆற்றல் குறைந்த வெப்பமான உடலின் மூலக்கூறுகளுக்கு மாற்றப்படுகிறது.
வெப்பத்திற்கும் வேலைக்கும் இடையிலான பொதுவான விஷயம் என்னவென்றால், அவை செயல்பாட்டின் செயல்பாடுகளாகும், அதாவது கணினி முதல் நிலையிலிருந்து இரண்டாவது நிலைக்கு மாறும்போது வெப்பம் மற்றும் வேலையின் அளவைப் பற்றி பேசலாம். வெப்பமும் வெப்பமும் உள் ஆற்றலைப் போலல்லாமல், மாநிலத்தின் செயல்பாடு அல்ல. நிலை 1 இல் உள்ள வாயுவின் வேலை மற்றும் வெப்பம் எதற்கு சமம் என்று சொல்ல முடியாது, ஆனால் நிலை 1 இல் உள்ள உள் ஆற்றலைப் பற்றி பேசலாம்.
§3நான்வெப்ப இயக்கவியலின் ஆரம்பம்
உள் ஆற்றலைக் கொண்ட ஒரு குறிப்பிட்ட அமைப்பு (பிஸ்டனின் கீழ் சிலிண்டரில் மூடப்பட்டிருக்கும்) ஒரு குறிப்பிட்ட அளவு வெப்பத்தைப் பெற்றுள்ளது என்று வைத்துக்கொள்வோம்.கே, ஒரு புதிய நிலைக்குச் செல்வது, உள் ஆற்றலால் வகைப்படுத்தப்படுகிறதுயு 2
,
வேலை செய்தார் ஏவெளிப்புற சூழலுக்கு மேலே, அதாவது வெளிப்புற சக்திகளுக்கு எதிராக. வெப்பத்தின் அளவு கணினிக்கு வழங்கப்படும் போது நேர்மறையாகவும், கணினியிலிருந்து எடுக்கப்படும் போது எதிர்மறையாகவும் கருதப்படுகிறது. வெளிப்புற சக்திகளுக்கு எதிராக வாயு மூலம் வேலை செய்யும்போது நேர்மறையாகவும், வாயுவில் செய்யப்படும் போது எதிர்மறையாகவும் இருக்கும்.
நான்வெப்ப இயக்கவியலின் ஆரம்பம் : வெப்ப அளவு (Δகே ), அமைப்பின் உள் ஆற்றலை அதிகரிக்கவும், வெளிப்புற சக்திகளுக்கு எதிராக அமைப்பின் மூலம் வேலை (A) செய்யவும் பயன்படுத்தப்படுகிறது.
பதிவு நான்வேறுபட்ட வடிவத்தில் வெப்ப இயக்கவியலின் ஆரம்பம்
dU- அமைப்பின் உள் ஆற்றலில் எல்லையற்ற மாற்றம்
தொடக்கப் பணி,- எல்லையற்ற சிறிய அளவு வெப்பம்.
கணினி அவ்வப்போது அதன் அசல் நிலைக்குத் திரும்பினால், அதன் உள் ஆற்றலில் ஏற்படும் மாற்றம் பூஜ்ஜியமாகும். பிறகு
அதாவது நிரந்தர இயக்க இயந்திரம்நான்ஒரு குறிப்பிட்ட கால இடைவெளியில் இயங்கும் இயந்திரம், வெளியில் இருந்து கொடுக்கப்படும் ஆற்றலை விட அதிக வேலைகளைச் செய்யும் என்பது சாத்தியமற்றது (சூத்திரங்களில் ஒன்றுநான்வெப்ப இயக்கவியலின் ஆரம்பம்).
§2 ஒரு மூலக்கூறின் சுதந்திரத்தின் டிகிரி எண்ணிக்கை. சீருடை பற்றிய சட்டம்
மூலக்கூறின் சுதந்திரத்தின் அளவுகளில் ஆற்றல் விநியோகம்
சுதந்திரத்தின் அளவுகளின் எண்ணிக்கை: ஒரு இயந்திர அமைப்பு என்பது அமைப்பின் நிலையைக் குறிப்பிடக்கூடிய சுயாதீன அளவுகளின் எண்ணிக்கையாகும். மோனாடோமிக் வாயு மூன்று மொழிமாற்ற டிகிரி சுதந்திரத்தைக் கொண்டுள்ளதுநான் = 3, விண்வெளியில் அத்தகைய வாயுவின் நிலையை விவரிக்க, மூன்று ஆயங்கள் (x, y, z).
கடினமான டைஅணுக்களுக்கு இடையிலான தூரம் மாறாத பிணைப்பு என்று அழைக்கப்படுகிறது. ஒரு திடமான பிணைப்பைக் கொண்ட டயட்டோமிக் மூலக்கூறுகள் (என் 2 , ஓ 2 , N 2) 3 மொழியாக்க டிகிரி சுதந்திரம் மற்றும் 2 சுழற்சி டிகிரி சுதந்திரம்:நான்= நான்வேகமாக + நான்vr=3 + 2=5.
சுதந்திரத்தின் மொழிபெயர்ப்பு அளவுகள் விண்வெளியில் மூலக்கூறின் ஒட்டுமொத்த இயக்கத்துடன் தொடர்புடையது, சுழற்சி - ஒட்டுமொத்தமாக மூலக்கூறின் சுழற்சியுடன். தொடர்புடைய ஒருங்கிணைப்பு அச்சுகளின் சுழற்சிஎக்ஸ்மற்றும் zஒரு கோணத்தில் அச்சில் சுழலும் போது விண்வெளியில் மூலக்கூறுகளின் நிலையில் மாற்றம் ஏற்படும் மணிக்குமூலக்கூறு அதன் நிலையை மாற்றாது, எனவே, ஒருங்கிணைப்பு φ ஒய்இந்த வழக்கில் தேவையில்லை. இறுக்கமான பிணைப்பைக் கொண்ட ஒரு முக்கோண மூலக்கூறு 6 டிகிரி சுதந்திரத்தைக் கொண்டுள்ளது
நான்= நான்வேகமாக + நான்vr=3 + 3=6
அணுக்களுக்கு இடையிலான பிணைப்பு இறுக்கமாக இல்லாவிட்டால், அதிர்வுஉடன் சுதந்திரத்தின் அளவுகள். நேரியல் அல்லாத மூலக்கூறுக்குமற்றும் எண்ணவும் . = 3 என் - 6 , எங்கே என்- ஒரு மூலக்கூறில் உள்ள அணுக்களின் எண்ணிக்கை.
மூலக்கூறுகளின் சுதந்திரத்தின் மொத்த எண்ணிக்கையைப் பொருட்படுத்தாமல், 3 டிகிரி சுதந்திரம் எப்போதும் மொழிபெயர்ப்பாகும். மொழிபெயர்ப்புப் பட்டங்கள் எதுவும் மற்றவற்றை விட ஒரு நன்மையைக் கொண்டிருக்கவில்லை, எனவே அவை ஒவ்வொன்றும் சராசரியாக ஒரே ஆற்றலைக் கொண்டுள்ளன, மதிப்பின் 1/3 க்கு சமம்
![]()
போல்ட்ஸ்மேன் ஒரு சட்டத்தை நிறுவினார், அதன் படி ஒரு புள்ளிவிவர அமைப்புக்கு (அதாவது, மூலக்கூறுகளின் எண்ணிக்கை அதிகமாக இருக்கும் ஒரு அமைப்புக்கு), இது வெப்ப இயக்கவியல் சமநிலை நிலையில் உள்ளது, ஒவ்வொரு மொழிபெயர்ப்பு மற்றும் சுழற்சி அளவு சுதந்திரத்திற்கும் சராசரி இயக்கவியல் உள்ளது. ஆற்றல் 1/2 க்கு சமம் kT , மற்றும் ஒவ்வொரு அதிர்வு அளவிலான சுதந்திரத்திற்கும் - சராசரியாக, ஆற்றல் சமமாக இருக்கும் kT . சுதந்திரத்தின் அதிர்வு அளவு இரண்டு மடங்கு ஆற்றலைக் கொண்டுள்ளது, ஏனெனில் இது இயக்க ஆற்றலை (மொழிபெயர்ப்பு மற்றும் சுழற்சி இயக்கத்தைப் போல) மட்டுமல்ல, சாத்தியமான ஆற்றலுக்கும் காரணமாகிறது.இதனால் ஒரு மூலக்கூறின் சராசரி ஆற்றல்
ஒரு சிறந்த வாயுவின் மூலக்கூறுகள் ஒன்றுக்கொன்று தொடர்பு கொள்ளாது, எனவே, ஆற்றல் இல்லை. எனவே, சிறந்த வாயு மூலக்கூறுகளின் அனைத்து ஆற்றலும் மொழிபெயர்ப்பு மற்றும் சுழற்சி இயக்கங்களின் இயக்க ஆற்றலை மட்டுமே கொண்டுள்ளது. முந்தைய பத்தியில் [சூத்திரம் (17)] மூலக்கூறின் மொழிபெயர்ப்பு இயக்கத்தின் சராசரி இயக்க ஆற்றலை நாங்கள் தீர்மானித்தோம். ஒரு மூலக்கூறின் சுழற்சி இயக்கத்தின் சராசரி இயக்க ஆற்றலை கணக்கில் எடுத்துக்கொள்வதற்கு, உடலின் சுதந்திரத்தின் டிகிரி எண்ணிக்கையின் கருத்தை கருத்தில் கொள்வது அவசியம்.
ஒரு உடலின் சுதந்திரத்தின் டிகிரி எண்ணிக்கை என்பது விண்வெளியில் உடல்களின் நிலையை தீர்மானிக்கும் சுயாதீன ஆயங்களின் எண்ணிக்கை.
இந்த வரையறையை விளக்குவோம். ஒரு உடல் விண்வெளியில் முற்றிலும் தன்னிச்சையாக நகர்ந்தால், இந்த இயக்கம் எப்போதும் ஆறு ஒரே நேரத்தில் சுயாதீனமான இயக்கங்களால் ஆனது: மூன்று மொழிபெயர்ப்பு (ஒரு செவ்வக ஒருங்கிணைப்பு அமைப்பின் மூன்று அச்சுகளுடன்) மற்றும் மூன்று சுழற்சி (சுமார் மூன்று பரஸ்பர செங்குத்து அச்சுகள் ஈர்ப்பு மையத்தின் வழியாக செல்கின்றன. உடல்) (படம் 75). வேறு வார்த்தைகளில் கூறுவதானால், விண்வெளியில் உடலின் நிலை இந்த வழக்கில் ஆறு சுயாதீன ஆயங்களால் தீர்மானிக்கப்படுகிறது: மூன்று நேரியல் மற்றும் மூன்று கோணம். எனவே, வரையறையின்படி, விண்வெளியில் தன்னிச்சையாக நகரும் உடலின் சுதந்திரத்தின் டிகிரி எண்ணிக்கை ஆறு ( மூன்று மொழிபெயர்ப்பு மற்றும் மூன்று சுழற்சி டிகிரி சுதந்திரம்). ஒரு உடலின் இயக்க சுதந்திரம் குறைவாக இருந்தால், அதன் சுதந்திரத்தின் எண்ணிக்கை ஆறுக்கும் குறைவாக இருக்கும். எடுத்துக்காட்டாக, ஒரு உடல் ஒரு விமானத்தில் மட்டுமே நகர்கிறது, அதே நேரத்தில் தன்னிச்சையான சுழற்சி (ஒரு உருட்டல் பந்து) சாத்தியமாகும். அதன் சுதந்திர டிகிரிகளின் எண்ணிக்கை ஐந்து (இரண்டு மொழிபெயர்ப்பு மற்றும் மூன்று சுழற்சி). ஒரு ரயில்வே காருக்கு ஒரு அளவு சுதந்திரம் (மொழிபெயர்ப்பு) உள்ளது, ஏனெனில் அது பாதையில் மட்டுமே நகரும். வண்டிச் சக்கரம் இரண்டு டிகிரி சுதந்திரத்தைக் கொண்டுள்ளது: ஒரு மொழிபெயர்ப்பு (வண்டியுடன் சேர்ந்து) மற்றும் ஒரு சுழற்சி (கிடைமட்ட அச்சைச் சுற்றி).
வாயு மூலக்கூறின் இயக்க ஆற்றல் பற்றிய கேள்விக்கு இப்போது திரும்புவோம். மூலக்கூறுகளின் இயக்கத்தின் முழுமையான சீரற்ற தன்மை காரணமாக, அவற்றின் அனைத்து வகையான இயக்கங்களும் (மொழிபெயர்ப்பு மற்றும் சுழற்சி இரண்டும்) சமமாக சாத்தியமாகும் (சமமாக சாத்தியம்). எனவே, ஒரு மூலக்கூறின் ஒவ்வொரு அளவு சுதந்திரத்திற்கும், சராசரியாக, அதே அளவு ஆற்றல் உள்ளது (சுதந்திரத்தின் அளவுகளில் ஆற்றலின் சீரான விநியோகம் குறித்த போல்ட்ஸ்மேனின் தேற்றம்).
மூலக்கூறுகள் முற்றிலும் சீரற்ற முறையில் நகர்வதால், அவை ஆறு டிகிரி சுதந்திரத்தைக் கொண்டிருக்க வேண்டும். இருப்பினும், இங்கே நாம் பின்வரும் சூழ்நிலையை கணக்கில் எடுத்துக்கொள்ள வேண்டும்.
ஒரு மோனாடோமிக் வாயுவின் மூலக்கூறு (எடுத்துக்காட்டாக, அவர்) ஒரு பொருள் புள்ளியாகக் குறிப்பிடப்படலாம், அதன் சொந்த அச்சுகளைச் சுற்றி அதன் சுழற்சி விண்வெளியில் அதன் நிலையை மாற்றாது. இதன் பொருள் ஒரு மோனாடோமிக் மூலக்கூறின் நிலையை தீர்மானிக்க அதன் நேரியல் ஆயங்களை மட்டும் குறிப்பிடுவது போதுமானது. எனவே, ஒரு மோனாடோமிக் மூலக்கூறு மூன்று (மொழிபெயர்ப்பு) க்கு சமமான சுதந்திரத்தின் பல டிகிரிகளை ஒதுக்க வேண்டும். இயற்பியல் கண்ணோட்டத்தில், இந்த சூழ்நிலையை பின்வருமாறு விளக்கலாம். உடலின் சுழற்சி இயக்கத்தின் இயக்க ஆற்றல் (§ 23 ஐப் பார்க்கவும்) சமம்
![]()
சுழற்சியின் கோண வேகம் எங்கே, நான் உடலின் நிலைமத்தின் தருணம். ஒரு பொருள் புள்ளிக்கு
பொருள் புள்ளியின் நிறை எங்கே, சுழற்சியின் அச்சில் இருந்து அதன் தூரம். ஒரு பொருள் புள்ளி அதன் அச்சில் சுழன்றால், ஆனால் அதன் விளைவாக, ஒரு மோனடோமிக் மூலக்கூறுக்கு, சுழற்சி இயக்கம் (சுதந்திரத்தின் சுழற்சி அளவுகள்) எண்ணற்ற ஆற்றலைக் கணக்கிடுகிறது, இது புறக்கணிக்கப்படலாம். குவாண்டம் இயக்கவியலின் அடிப்படையில் மட்டுமே இந்த நிலைப்பாட்டின் கடுமையான ஆதாரம் சாத்தியமாகும்.

ஒரு டயட்டோமிக் வாயு மூலக்கூறு (உதாரணமாக, ) இரண்டு பொருள் புள்ளிகளின் தொகுப்பாகக் குறிப்பிடப்படலாம் - அணுக்கள், இரசாயன பிணைப்புகளால் ஒருவருக்கொருவர் கடுமையாக இணைக்கப்பட்டுள்ளன (படம் 76, a). இரண்டு அணுக்கள் வழியாகச் செல்லும் அச்சில் அத்தகைய மூலக்கூறின் சுழற்சி விண்வெளியில் மூலக்கூறின் நிலையை மாற்றாது. இயற்பியல் பார்வையில், அணுக்கள் வழியாகச் செல்லும் அச்சைச் சுற்றி ஒரு மூலக்கூறின் சுழற்சியுடன் தொடர்புடைய ஆற்றல் பூஜ்ஜியத்திற்கு அருகில் உள்ளது. எனவே, ஒரு டையடோமிக் மூலக்கூறுக்கு ஐந்து டிகிரி சுதந்திரம் (மூன்று மொழிபெயர்ப்பு மற்றும் இரண்டு சுழற்சி) ஒதுக்கப்பட வேண்டும்.
முக்கோண மூலக்கூறைப் பொறுத்தவரை (படம் 76, b), இது வெளிப்படையாக அனைத்து ஆறு டிகிரி சுதந்திரத்தையும் கொண்டுள்ளது (மூன்று மொழிபெயர்ப்பு மற்றும் மூன்று சுழற்சி). மற்ற பாலிடோமிக் மூலக்கூறுகள் (டெட்ராடோமிக், பென்டாடோமிக், முதலியன) சுதந்திரத்தின் அதே எண்ணிக்கையில் உள்ளன.
ஒரு மூலக்கூறின் சுதந்திரத்தின் ஒரு டிகிரிக்கு சராசரி இயக்க ஆற்றலைக் கணக்கிட, நாம் சூத்திரத்தைப் பயன்படுத்துகிறோம் (17):
இந்த ஆற்றல் மூன்று டிகிரி சுதந்திரம் கொண்ட ஒரு மோனாடோமிக் மூலக்கூறுக்கு (ஒரு பொருள் புள்ளியாக) பெறப்பட்டதால், மூலக்கூறின் ஒரு டிகிரி சுதந்திரத்திற்கு ஆற்றல் உள்ளது.
![]()
பின்னர், குறிப்பிடப்பட்ட போல்ட்ஸ்மேன் தேற்றத்தின்படி, சுதந்திரத்தின் அளவுகளைக் கொண்ட ஒரு மூலக்கூறு மொத்த இயக்க ஆற்றலைக் கொண்டிருக்கும்.
![]()
இதன் விளைவாக, ஒரு வாயு மூலக்கூறின் மொத்த இயக்க ஆற்றல் அதன் முழுமையான வெப்பநிலைக்கு விகிதாசாரமாகும் மற்றும் அதை மட்டுமே சார்ந்துள்ளது.
சூத்திரத்திலிருந்து (19) முழுமையான பூஜ்ஜிய வெப்பநிலையின் இயற்பியல் பொருளைப் பின்பற்றுகிறது: விருப்பப்படி, அதாவது முழுமையான பூஜ்ஜியத்தில், வாயு மூலக்கூறுகளின் இயக்கம் நிறுத்தப்படும்.
சூத்திரத்தின்படி (19), ஒரு மோனாடோமிக் மூலக்கூறு மொத்த ஆற்றலைக் கொண்டுள்ளது
![]()
ஒரு டையடோமிக் மூலக்கூறு மொத்த ஆற்றலைக் கொண்டுள்ளது
![]()
முக்கோண மற்றும் பாலிடோமிக் மூலக்கூறுகள் மொத்த ஆற்றலைக் கொண்டுள்ளன
![]()
ஒரு குறிப்பிட்ட வெகுஜன வாயுவின் உள் ஆற்றல் இந்த வெகுஜனத்தில் உள்ள மூலக்கூறுகளின் எண்ணிக்கை மற்றும் ஒரு மூலக்கூறின் மொத்த இயக்க ஆற்றலின் உற்பத்திக்கு சமம்:
![]()
ஒரு மோல் வாயுவிற்கு, மோலின் உள் ஆற்றலைப் பெறுகிறோம் (அதைக் கணக்கில் எடுத்துக்கொள்கிறோம்



